研究确定了致癌基因如何调节前列腺癌的遗传变异
来自伦敦玛丽女王大学巴茨癌症研究所 (BCI)、意大利基因组医学研究所和米兰大学的研究人员确定了致癌基因在控制支持前列腺遗传变异的重要遗传过程中的新作用癌症。
今天发表在《细胞报告》上的研究结果揭示了该基因如何影响前列腺癌中遗传变异的产生,这些变异可以预测疾病复发并代表新的药物靶点以提高患者的存活率。
共同资深作者、BCI 小组组长兼 Barts Health NHS Trust 泌尿外科顾问顾问 Prabhakar Rajan 博士说:“前列腺癌是世界上 [最常见的] 男性癌症,也是男性癌症相关死亡的主要原因。它“它的基因组成非常多变,这使得诊断和治疗变得棘手,因为没有一种万能的方法来治疗患者。了解基因变异的驱动因素将有助于我们更好地了解疾病,并改进治疗。”
选择性剪接是基因片段被改组以创建称为“剪接变体”的遗传密码的不同组合的过程,这些组合提供了制造蛋白质的指令。通过可变剪接,单个基因可以编码多种不同的蛋白质,这些蛋白质在细胞中表达水平不同,具有不同的功能。
选择性剪接是调节基因表达和在正常细胞内产生遗传和蛋白质多样性的重要过程;然而,它在许多癌症类型中被破坏,包括前列腺癌。
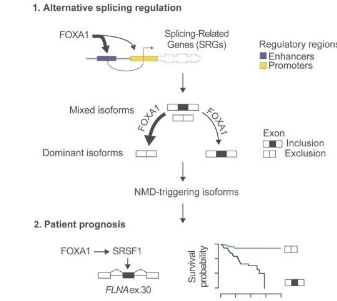
在这项研究中,研究小组发现致癌基因 FOXA1 是前列腺癌可变剪接的关键调节因子,并且可能控制影响疾病复发和患者生存的剪接变体的产生。
FOXA1 微调前列腺癌中的选择性剪接
FOXA1 是一种被称为先驱转录因子的蛋白质。转录因子可以选择 DNA 中的哪些基因被转录成用于在我们的细胞内制造蛋白质的指令以及这种情况发生的速率。作为先驱因子,FOXA1 为不同转录因子的结合打开了 DNA 。已发现 FOXA1 的变化会驱动前列腺癌的发生和进展。
通过评估细胞系模型和前列腺癌原发病例中的可变剪接,研究小组发现高水平的 FOXA1 限制了对癌细胞具有功能益处的剪接变体的遗传多样性。研究表明,FOXA1 有利于细胞内高水平存在的剪接变体,并沉默低水平表达的剪接变体,从而减少前列腺癌中的剪接变异性。
Rajan 博士说:“这一独特的发现以前从未在选择性剪接的控制器中得到证实,这可能意味着 FOXA1 指导前列腺癌细胞以可能对患者有害的特定方式发挥作用。”
共同资深作者、米兰大学副教授兼意大利基因组医学研究所小组组长 Matteo Cereda 教授补充说:“我们首次表明,转录调控的早期参与者也负责微调选择性剪接。”
潜在的新治疗目标
为了确定 FOXA1 控制的可变剪接是否对患者生存产生影响,该团队分析了来自 300 多名原发性前列腺癌患者的临床数据,这些数据可通过癌症基因组图谱获得。
尽管高水平的 FOXA1 降低了剪接变异性,但研究小组发现 FOXA1 增强了将遗传片段纳入剪接变体中,这些剪接变体是前列腺癌复发的强标志。使用前列腺癌细胞系,研究小组发现,在 FOXA1 控制的称为 FLNA 基因的基因的剪接变体中包含一个特定的遗传片段,赋予前列腺癌细胞生长优势,这可能会导致早期疾病复发.
Rajan 博士说:“这项研究说明了我们如何利用基因组学的力量就如何控制前列腺癌的遗传变异性做出重要的科学发现。我们希望我们的研究结果能够通过识别更精确的疾病复发标记和新的标记来产生临床影响。潜在的药物靶点。”
该团队现在希望进一步测试他们已确定与癌症复发相关的剪接变体是否可用于预测现实中的疾病复发,并进行实验以确定靶向这些基因是否可以代表治疗前列腺癌的新方法。
版权声明:本文由用户上传,如有侵权请联系删除!
