一种无炎症副作用的阿尔茨海默氏症新药
尽管 Aduhelm 是一种靶向淀粉样蛋白 β (Aβ) 的单克隆抗体,基于其降低 AD 患者 Aβ 斑块负担的能力,最近成为 FDA 批准的首个治疗阿尔茨海默病 (AD) 的药物,但其对认知改善的作用仍存在争议。
此外,大约 40% 接受这种抗体治疗的患者出现严重的副作用,包括脑水肿 (ARIA-E) 和出血 (ARIA-H),这些副作用可能与 Aβ 抗体结合 Fc 受体 (FCR) 时大脑中的炎症反应有关) 免疫细胞,如小胶质细胞和巨噬细胞。这些炎症副作用可导致神经元细胞死亡和激活的小胶质细胞消除突触,甚至有可能加剧 AD 患者的认知障碍。因此,目前基于 Aβ 抗体的免疫疗法由于其炎症副作用而存在弊大于利的固有风险。
为了克服这些问题,韩国 KAIST 的一组研究人员开发了一种新型融合蛋白药物 αAβ-Gas6,它通过与基于 Aβ 抗体的免疫疗法完全不同的机制有效消除 Aβ。在 AD 小鼠模型中,αAβ-Gas6 不仅以更高的效力去除了 Aβ,而且还规避了与常规抗体治疗相关的神经毒性炎症副作用。
他们的研究结果发表在 8 月 4 日的《自然医学》杂志上。
“通过 Aβ 靶向抗体激活 FcR 会诱导小胶质细胞介导的 Aβ 吞噬作用,但它也会产生炎症信号,不可避免地损害脑组织,”论文作者、KAIST 生物科学系副教授 Chan Hyuk Kim 和 Won-Suk Chung 说。
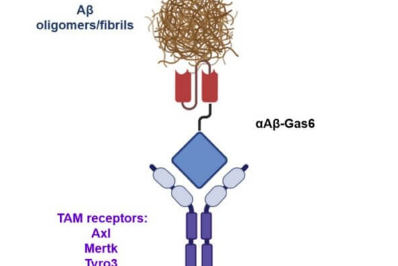
“因此,我们利用了胞吐作用,这是一种细胞过程,通过吞噬细胞去除死细胞作为清除大脑中 Aβ 的替代途径,”Kim 和 Chung 教授说。“细胞增多症伴随着维持组织稳态的抗炎反应。为了利用这一过程,我们设计了 Gas6,这是一种可溶性衔接蛋白,可通过 TAM 吞噬受体介导胞吐作用,使其靶标特异性从死细胞重定向到 Aβ 斑块。”
教授和他们的团队证明,由此产生的 αAβ-Gas6 通过激活小胶质细胞和星形细胞吞噬作用诱导 Aβ 吞噬,因为 TAM 吞噬受体在大脑中的这两个主要吞噬细胞中高度表达。重要的是,αAβ-Gas6 促进了 Aβ 的强烈摄取,而没有显示任何炎症和神经毒性迹象,这与使用 Aβ 单克隆抗体的治疗形成鲜明对比。此外,他们发现 αAβ-Gas6 显着减少了小胶质细胞对突触的过度消除,从而导致 AD 模型小鼠的行为得到更好的拯救。
“通过使用脑淀粉样血管病 (CAA) 的小鼠模型,这是一种由 Aβ 在脑血管壁内沉积引起的脑血管疾病,我们还表明,Gas6 融合蛋白的鞘内给药显着消除了脑血管淀粉样蛋白,以及减少微出血。这些数据表明,aAb-Gas6 是一种有效的治疗剂,可以消除 Aβ,而不会加剧 CAA 相关的微出血。”
Kim 和 Chung 教授指出:“我们相信我们的方法可以在治疗 AD 方面取得突破,而不会引起炎症副作用和突触丢失。我们的方法有望成为一种适用于 AD 以外的新型治疗平台。通过改变融合蛋白的靶向特异性,Gas6融合蛋白可应用于各种神经系统疾病以及受有毒分子影响的自身免疫性疾病,这些分子应在不引起炎症反应的情况下去除。”
Kim 和 Chung 教授基于设计嵌合 Gas6 融合蛋白的策略创立了“Illimis Therapeutics”,该融合蛋白可以去除神经系统中的有毒聚集体。通过这家公司,他们计划进一步开发各种 Gas6 融合蛋白,不仅用于 Ab,还用于 Tau 治疗 AD 症状。
这项工作得到了 KAIST 和由韩国健康产业发展研究所 (KHIDI) 和韩国痴呆症研究中心 (KDRC) 管理的韩国健康技术研发项目的支持,该中心由卫生与福利部 (MOHW) 和韩国部资助科学与信息通信技术 (MSIT) 和 KAIST。
其他贡献者包括 Hyuncheol Jung 和 Se Young Lee、Sungjoon Lim、Hyeong Ryeol Choi、Yeseong Choi、Minjin Kim、Segi Kim、生物科学系和韩国科学技术高等研究院 (KAIST)。
版权声明:本文由用户上传,如有侵权请联系删除!
