创造具有增强抗癌活性的新型氨基酸纳米颗粒
酪氨酸和色氨酸等氨基酸是构成蛋白质的基本组成部分。这些生物分子的每个末端和侧链上都有不同的化学基团,因此具有通过形成酰胺(肽)键形成链的天然能力。然而,这种连接很弱并且在生理条件下很容易降解。这就是 Fmoc 保护的氨基酸发挥作用的地方。
在一项新的研究中,由先进科学技术研究所 (JAIST) 副教授 Eijiro Miyako 博士以及国家科学研究中心的 Alberto Bianco 博士和 Cécilia Ménard-Moyon 博士领导的研究小组(法国 CNRS)采用 254 nm 的紫外线(产生 CBPUV 纳米颗粒)和 365 nm 的核黄素介导的交联(产生 CBPRibo 纳米颗粒)来交联 Fmoc 保护的氨基酸。“氨基酸作为蛋白质的组成部分具有许多优点,例如更好的生物相容性。因此,我们希望创造出新型自组装氨基酸纳米颗粒,它可以通过多种机制触发,” Eijiro Miyako 博士在解释他们研究背后的动机时说道。这项研究的结果发表在《Small》杂志上。
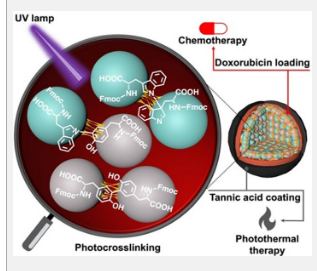
自组装的氨基酸是Fmoc-Tyr-OH(酪氨酸)和Fmoc-Trp-OH(色氨酸)稳定交联的二聚体。随后将抗癌药物阿霉素负载到交联氨基酸纳米颗粒中。为了提高纳米粒子的稳定性,研究人员使用单宁酸-铁(Fe 3+)络合物(或TAF)作为涂层的外层。这种涂层可以通过谷胱甘肽酶促释放或肿瘤微环境中的 pH 差异在细胞内降解。单宁酸涂层还可用于光热抗癌疗法,其中外部光可以增加癌组织周围的局部温度,导致癌细胞亡。
然后对合成的纳米颗粒的结构完整性、稳定性和不同 pH 条件下的药物释放进行了广泛的研究。然后使用细胞培养技术研究自组装氨基酸纳米粒子的功能特征、细胞摄取和生物相容性。最后,在荷瘤小鼠中分析了合成纳米颗粒的抗癌功效。利用阿霉素作用的化疗和利用单宁酸涂层的光热疗法的组合方法显示出优异的抗癌活性。
交联后,基于氨基酸的纳米粒子在颜色、尺寸、吸光度、荧光和热稳定性方面表现出显着的变化。此外,与 CBPRibo 相比,CBPUV 在交联后表现出优异的稳定性。CBPUV 也始终保持其结构,而 CBPRibo 则显示出部分分解,形成空心球体。药物释放研究表明,在生理 pH (7.4) 下药物释放极少,表明稳定的涂层对于体内递送至关重要。在 pH 5.5 时,不完全的涂层降解导致药物释放可以忽略不计。然而,在 pH 5.5 下添加谷胱甘肽 (GSH) 通过触发 TAF 涂层降解,显着促进了药物释放,表明 GSH/pH 响应。酸性和 GSH 联合处理加剧了涂层降解。这种响应行为能够在特定的生理条件下控制药物的释放。此外,体外评估揭示了浓度依赖性细胞性,并提高了联合化疗/光热疗法的疗效。对荷瘤小鼠的体内研究显示出显着的肿瘤生长抑制作用,表明具有良好的抗癌作用,且没有观察到副作用。
Miyako 博士分享了他对研究结果的总结性想法,他说:“纳米技术有望将基础实验室科学转变为对抗癌症等复杂疾病的强大工具。我们乐观地认为,这项开创性的研究将取得进展,有可能在十年内发展成为尖端的癌症治疗技术,为临床试验做好准备。”
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
