显微镜技术揭示了细胞和组织中隐藏的纳米结构
在活细胞内部,蛋白质和其他分子通常紧密地挤在一起。这些致密的簇可能很难成像,因为用于使它们可见的荧光标记不能将自己楔入分子之间。
麻省理工学院的研究人员现在已经开发出一种新颖的方法来克服这种限制,并使那些“不可见”的分子可见。他们的技术允许他们在标记分子之前通过扩展细胞或组织样品来“分散”分子,这使得分子更容易被荧光标签所接受。
这种方法建立在麻省理工学院以前开发的一种广泛使用的称为膨胀显微镜的技术之上,应该允许科学家可视化以前从未见过的分子和细胞结构。
“越来越清楚的是,扩张过程将揭示许多新的生物学发现。如果生物学家和临床医生一直在研究大脑中的蛋白质或其他生物标本,并且他们以常规方式对其进行标记,他们可能会错过整个类别的现象,“Y. Eva Tan神经技术教授,麻省理工学院生物工程和大脑与认知科学教授爱德华博伊登说,他是霍华德休斯医学研究所的研究员, 也是麻省理工学院麦戈文脑研究所和科赫综合癌症研究所的成员。
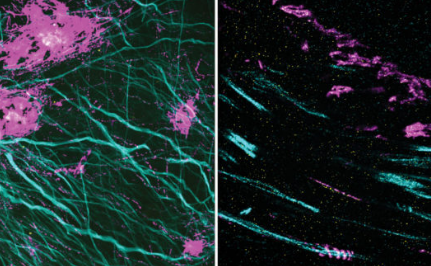
使用这种技术,Boyden和他的同事们表明,他们可以成像神经元突触中发现的纳米结构。他们还比以前更详细地对阿尔茨海默氏症连接的淀粉样蛋白β斑块的结构进行了成像。
“我们的技术,我们称之为扩展揭示,能够可视化这些纳米结构,这些纳米结构以前仍然是隐藏的,使用学术实验室容易获得的硬件,”媒体实验室的助理教授,该研究的主要作者之一Deblina Sarkar说。
去拥挤
对细胞内的特定蛋白质或其他分子进行成像需要用与靶标结合的抗体携带的荧光标签对其进行标记。抗体长约10纳米,而典型的细胞蛋白通常直径约2至5纳米,因此,如果靶蛋白堆积太稠密,抗体就无法到达它们。
这一直是传统成像的障碍,也是Boyden于2015年首次开发的膨胀显微镜的原始版本的障碍。在原始版本的膨胀显微镜中,研究人员在感兴趣的分子膨胀组织之前将荧光标记贴在它们身上。首先进行标记,部分原因是研究人员必须使用酶来切碎样品中的蛋白质,以便组织可以膨胀。这意味着蛋白质在组织扩增后无法标记。
为了克服这个障碍,研究人员必须找到一种方法来扩大组织,同时保持蛋白质完整。他们使用热量而不是酶来软化组织,使组织膨胀20倍而不会被破坏。然后,分离的蛋白质可以在扩增后用荧光标签标记。
随着如此多的蛋白质可用于标记,研究人员能够识别突触内的微小细胞结构,突触是密集富含蛋白质的神经元之间的连接。他们标记并成像了七种不同的突触蛋白,这使他们能够详细地可视化由与其他突触蛋白对齐的钙通道组成的“纳米列”。这些纳米列被认为有助于提高突触通信效率,由Blanpied的实验室于2016年首次发现。
“这项技术可以用来回答很多关于突触蛋白功能障碍的生物学问题,突触蛋白与神经退行性疾病有关,”Kang说。“到目前为止,还没有工具可以很好地可视化突触。
新模式
研究人员还使用他们的新技术对β淀粉样蛋白进行成像,这是一种在阿尔茨海默氏症患者大脑中形成斑块的肽。利用来自小鼠的脑组织,研究人员发现β淀粉样蛋白形成周期性纳米团簇,这是以前从未见过的。这些β淀粉样蛋白簇还包括钾通道。研究人员还发现了沿轴突形成螺旋结构的β淀粉样蛋白分子。
“在这篇论文中,我们没有推测这种生物学可能意味着什么,但我们证明了它的存在。这只是我们可以看到的新模式的一个例子,“麻省理工学院的研究生玛格丽特施罗德说,他也是这篇论文的作者。
Sarkar说,她对这项技术揭示的纳米级生物分子图案着迷。“凭借纳米电子学的背景,我在纳米晶圆厂中开发了需要极其精确对准的电子芯片。但是,当我看到在我们的大脑中,大自然母亲以如此纳米级的精度排列生物分子时,这真的让我大吃一惊,“她说。
Boyden和他的小组成员现在正在与其他实验室合作研究细胞结构,例如与帕金森氏症和其他疾病相关的蛋白质聚集体。在其他项目中,他们正在研究感染参与大脑衰老的细胞和分子的病原体。博伊登说,这些研究的初步结果也揭示了新的结构。
“一次又一次,你看到真正令人震惊的事情,”他说。“它向我们展示了我们在经典的未扩展染色方面缺少了多少。
研究人员还致力于修改该技术,以便他们可以一次成像多达20种蛋白质。他们还在努力调整他们的过程,以便它可以用于人体组织样本。
另一方面,Sarkar和她的团队正在开发可以分布在大脑中的微型无线供电纳米电子设备。他们计划将这些设备与扩展揭示集成在一起。“这可以将纳米电子学的智能与扩展技术的纳米镜能力相结合,对大脑进行综合功能和结构理解,”Sarkar说。
版权声明:本文由用户上传,如有侵权请联系删除!
