免疫系统在造血干细胞的生成过程中发挥着关键的一步
一种有助于识别和对抗细菌感染的微生物传感器在造血干细胞的发育中也发挥着关键作用,这为创造患者来源的造血干细胞、消除骨髓移植的需要提供了宝贵的新见解。 。
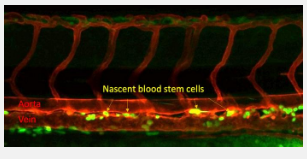
爱荷华州立大学遗传学、发育和细胞生物学助理教授 Raquel Espin Palazon 领导的研究小组的这一发现于上个月发表在《自然通讯》上。它建立在 Espin Palazon 之前的研究基础上,该研究表明,当血管系统和血液在胚胎中形成时,促进人体免疫反应的炎症信号在生命的最早阶段具有完全不同的作用。
Espin Palazon 表示,了解胚胎会激活微生物传感器(一种名为 Nod1 的蛋白质),迫使血管内皮细胞变成造血干细胞,可能有助于开发一种在实验室中利用患者自身血液制造造血干细胞的方法。
她说:“这将消除寻找相容的骨髓移植捐献者的挑战性任务以及接受移植后发生的并发症,从而改善许多白血病、淋巴瘤和贫血患者的生活。”
关键提示
干细胞既是身体的工厂,也是身体的原材料,反复分裂以自我更新并为特定组织构建新细胞。胚胎中的多能干细胞可以产生人体所需的任何类型的细胞,而成体干细胞仅限于产生特定类型的细胞。血液干细胞,也称为造血干细胞,产生血液的所有成分。终生供应的造血干细胞是在胚胎出生前产生的。
Espin Palazon 的 团队 在内皮细胞开始转变为干细胞之前在胚胎中发现了免疫受体的激活,从而为这一转变做好了准备。
“我们知道血液干细胞是由内皮细胞形成的,但使细胞转换身份的因素却是个谜,”她说。“我们不知道需要这种受体,也不知道这么早就需要它,甚至在血液干细胞形成之前。”
研究人员通过分析人类胚胎的公共数据库来锁定Nod1,并使用斑马鱼进行研究,斑马鱼与人类有大约70%的基因组相同。造血干细胞的生成与 Nod1 水平密切相关,因为它的作用被抑制或增强。
为了证实Nod1也在人类血液发育中发挥作用,研究小组与费城儿童医院合作。那里的研究人员培育出了人类诱导多能干细胞,这些干细胞是从成熟样本中产生的,但经过基因重新编程,使其表现得像胚胎中发现的无所不能的干细胞一样。诱导多能干细胞可以产生大多数类型的血细胞,但不能产生功能性造血干细胞。但当研究人员拿走 Nod1 时,血液生成就会减弱,就像斑马鱼的造血干细胞一样。
寻找自体干细胞
对于希望设计一种从人类样本中产生造血干细胞的系统的科学家来说,弄清楚Nod1是造血干细胞发育的先决条件是一个进步,这可能为患有血液疾病的患者提供革命性的新选择。患者可以使用源自自身身体的干细胞进行治疗,而不是通过骨髓移植来挽救生命。骨髓是骨骼的海绵状内部,含有人体的大部分造血干细胞。自体干细胞可以避免移植物抗宿主病的风险,这是一种常见且可能致命的反应,当患者的免疫系统将移植物视为受到攻击的威胁时就会发生这种反应。
“这将是再生医学的巨大进步,”埃斯平·帕拉松说。
Espin Palazon 的团队正在继续解开造血干细胞产生的复杂相互作用,包括完善时间线。了解信号何时表达对于开发制造造血干细胞的方法至关重要。
“时机非常关键。这就像当你做饭时,你需要按照特定的顺序添加配料,”她说。
进一步的研究将受益于与费城儿童医院的合作,该医院对该研究的合著者之一——遗传学、发育和细胞生物学兼职助理教授克莱德·坎贝尔(Clyde Campbell)进行了有关创建诱导多能干细胞的方案的培训。
“我在爱荷华州立大学的团队将继续努力实现没有血液疾病的生活。我相信我们的研究将为最终创造治疗级血液干细胞来治愈血液疾病患者铺平道路,”Espin Palazon 说。
除了埃斯平·帕拉松和坎贝尔之外,爱荷华州立大学这项研究的其他合著者还包括第一作者程晓义,他是一名研究生;Karin Dorman,遗传学、发育和细胞生物学教授兼 Dale D. Grosvenor 主席;研究生 Masuma Khatun Usha 和 Rodolfo Calderon;助理研究员伊丽莎白·斯内拉;和前本科生阿比盖尔·戈登。爱丁堡大学的 Antonella Fidanza 以及费城儿童医院的 Giulia Pavani、Deborah French 和 Paul Gadue 也对这项工作做出了贡献。
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
