酶疗法显示出对儿童痴呆症的希望
对一种导致儿童痴呆和早逝的罕见神经系统疾病的研究强调了一种可能的治疗方法。
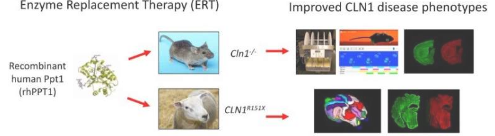
定期输注一种在患有婴儿巴顿病(也称为 CLN1 病)的儿童中缺乏的关键酶,可以改善患有同等遗传疾病的小鼠和绵羊。
由爱丁堡大学罗斯林研究所和圣路易斯华盛顿大学医学院领导的一项研究的研究结果可以为患有这种疾病的儿童开发有效的治疗方法,这可能导致视力丧失、认知和运动功能障碍、癫痫发作和早逝。
酶输液
科学家们研究了在具有相同缺陷基因的小鼠和绵羊中施用一定剂量的酶(称为 PPT1)的效果,这种缺陷基因会导致儿童患病。
每月向小鼠大脑注射 PPT1 酶可改善运动功能,减少脑细胞疾病迹象,并在六个月的治疗中减少脑物质损失。
研究小组首先验证了对小鼠产生有益作用所需的酶剂量和给药途径,并推断他们的发现以确定受影响绵羊的有效酶输注治疗方法。
这一关键步骤表明,在老鼠身上有希望的治疗可以扩大到在更大的大脑中产生类似的积极治疗效果。
细化
他们的研究建立在针对不同形式的 Batten 病(称为 CLN2)的类似方法之上,这导致了一种称为 cerliponase alfa 或 Brineura 的疗法。在世界各地的中心合作成功进行临床试验后,这已获得 NHS 的批准。
使用老鼠和绵羊的最新研究通过在老鼠身上测试基本原理,然后在大脑大小和复杂性与儿童相当的哺乳动物中对其进行改进,从而深入了解了治疗的效果。
研究小组希望进行进一步的研究,以完善酶替代疗法的有效时机和剂量,从而朝着对这种毁灭性儿童疾病的有效治疗迈进。
基因组编辑
巴顿病是称为溶酶体贮积症的几种疾病之一,是一组由影响细胞废物处理和回收系统的基因突变引起的神经退行性疾病的总称。
这些情况可能出现在儿童的不同阶段,具体取决于哪个基因缺陷。该疾病的 PPT1 缺陷型 CLN1 形式在儿童早期发展,进展迅速,目前没有可用的治疗方法。
Roslin 团队使用基因组编辑技术 CRISPR/Cas9 开发了一种针对这种疾病的绵羊模型,以便可以进行此类治疗研究。
这使研究人员能够更好地了解支持疾病进展的机制,并评估治疗疾病的新方法。这些动物在儿童身上表现出许多疾病的特征,从细胞疾病的迹象到大脑大小的变化。
该研究发表在《临床研究杂志》上。
“这项研究只能由一个合作研究团队完成。这项工作是朝着每个人的最终目标迈出的关键一步,即安全地对受这种破坏性疾病影响的儿童的潜在治疗方法进行临床试验。通过对绵羊的研究,我们获得了宝贵的见解研究这种情况的进展,这可以指导我们开发有效疗法的工作,”爱丁堡大学罗斯林研究所分子解剖学教授 Tom Wishart 说。
“我们与罗斯林研究所的同事一起工作,展示了这种新疗法治疗这种毁灭性致命疾病的潜力。我们不仅改善了小鼠的疾病,而且成功地将其扩大到在更大范围内具有相似的部分疗效。相同疾病的绵羊大脑模型。这是结合我们的专业知识,使用专门制作的模型来测试这种疗法的结果。我们的目标是能够治疗儿童患有这种疾病,这是实现这一目标的重要一步,”圣路易斯华盛顿大学医学院儿科、遗传学和神经学教授乔纳森·D·库珀博士说
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
