关键遗传密码变化驱动常见肺癌类型
由 NYU Langone Health 的 Perlmutter 癌症中心的研究人员领导的一个团队已经确定了一种基因,该基因可以促进第二种最常见类型肺癌的发展,从而更深入地了解如何治疗这种疾病。
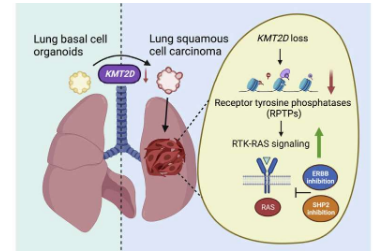
目前尚无针对肺鳞癌 (LUSC) 的经批准的靶向一线治疗,LUSC 是一种在器官内壁细胞层中形成的癌症,占肺癌死亡人数的 20% 至 30%。发表在Cancer Cell上的一项新研究发现,删除一个名为 KMT2D 的基因会导致在称为类器官的复杂培养物中生长的正常(基础)肺细胞转化为 LUSC 细胞。
根据研究作者的说法,KMT2D 调节能够构建蛋白酪氨酸磷酸酶的基因的活性,这些酶抑制通过称为受体酪氨酸激酶 (RTK) 的另一种酶组发送的细胞生长促进信号。已知称为 EGFR 和 ERBB2 的两种 RTK 参与 RTK-RAS 信号通路的异常激活,其中分子开关“卡在开启模式”,导致细胞作为癌症的一部分不断繁殖。
“我们的研究将 KMT2D 确定为肺鳞癌发展的关键因素,并提供了关于如何靶向 KMT2D 缺陷型 LUSC 的重要线索,”共同通讯作者 Kwok Kin-Wong 博士说,他是该研究所所长。 NYU Langone Health 血液学和肿瘤内科。“导致该基因导致癌症的相同遗传变化也会产生对靶向相关途径的现有药物非常敏感的肿瘤。”
建议的新方法
这项新研究证实了之前的证据,即 KMT2D 基因编码一种蛋白质(一种组蛋白甲基转移酶),这种蛋白质决定了酪氨酸磷酸酶基因在多大程度上可以被试图读取它们的细胞机器访问。
鉴于新研究对 LUSC 机制有了更好的理解,研究团队选择在研究小鼠中测试两种药物的组合——SHP2 抑制剂 SHP099 和泛 ERBB 抑制剂阿法替尼。
ERBB 因 KMT2D 信号缺陷而变得更加活跃,而酶 SHP 开启了 RTK-KAS 通路,就像 EGFR 和 ERBB2 一样,它们因缺乏 KMT2D 而变得更加活跃。该团队推断,当与 ERBB 抑制剂一起使用时,旨在抑制 SHP 的实验药物也可能会抵消 KMT2D 缺陷的影响。
事实上,他们发现这种组合减缓了患有 LUSC 的小鼠的肺肿瘤生长,这些小鼠被设计为缺乏 KMT2D,以及来自具有 KMT2D 突变的人类 LUSC 肿瘤的小鼠的肿瘤。
“多种 SHP2 抑制剂目前正在临床试验中进行测试,阿法替尼已经上市,”共同通讯作者张华医学博士说,他以前是纽约大学朗格健康中心医学系的讲师,现在是一名助理匹兹堡大学医学院和 UPMC 希尔曼癌症中心血液学和肿瘤学系医学系教授。“我们的研究结果保证了在患有 LUSC 的 KMT2D 缺陷患者中测试这些疗法 的临床试验的设计。”
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
