免疫细胞有后备机制
TBK1 酶是先天免疫系统的重要组成部分,在抵御病毒方面发挥着关键作用。在突变诱导的 TBK1 功能丧失后,患者表现出对病毒感染的易感性增加。引人注目的是,如果 TBK1 根本不表达,则看不到这种临床效果。波恩大学医院 Martin Schlee 教授和波恩大学 ImmunoSensation2 卓越集群的研究人员现在已经阐明了这种假设差异背后的机制。该研究发表在免疫学前沿杂志上。
在人体中,病毒颗粒被位于细胞内或细胞表面的所谓模式识别受体 (PRR) 识别。激活后,信号级联被初始化,最终导致信号分子如干扰素和细胞因子的产生和释放。这些信使分子提醒邻近的免疫细胞并指出病毒感染,从而引发免疫反应。
该信号级联的一部分是 TANK 结合激酶 1 (TBK1)。如果 PRR 检测到病毒颗粒,则 TBK1 会被激活。TBK1 反过来激活两个转录因子,它们进入细胞核,在那里它们诱导干扰素和细胞因子基因的转录。
对病毒感染的易感性
TBK1 基因的点突变可能导致 TBK1 功能丧失。在人类中,这表现为对病毒感染的临床易感性。引人注目的是,如果 TBK1 不表达并且在细胞中完全缺失,则不会观察到这种效果。“令人惊讶的是,人类完全没有 TBK1 表达与抗病毒反应降低无关,”波恩大学医院临床化学和临床药理学研究所的 Martin Schlee 教授说。到目前为止,尚不清楚为什么在免疫能力方面完全丧失 TBK1 表达比影响激酶功能的 TBK1 突变更能耐受。
波恩研究人员现在已经能够为这些以前无法解释的观察结果提供解释。“与 TBK1 非常相似的第二种酶在其中起着重要作用:IkB 激酶 epsilon,简称 IKKepsilon,”该研究的第一作者 Julia Wegner 博士解释道。就像 TBK1 一样,IKKepsilon 作用于 PRR 的下游并控制干扰素的表达。这两种蛋白质在结构上也非常相似,序列同源性超过 60%。一项新发现是 TBK1 对 IKKepsilon 有直接影响。“在骨髓细胞中,我们可以证明 TBK1 调节相关激酶 IKKepsilon 的表达,”Wegner 博士补充道。
没有半点措施
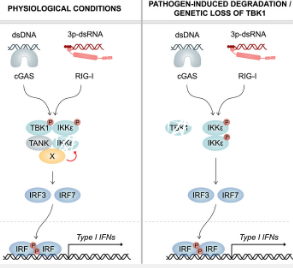
TBK1 降低了 IKKepsilon 的稳定性。这个过程与蛋白质的酶功能无关。“因此,由于点突变而失去功能的 TBK1 仍然能够破坏 IKKepsilon 的稳定性,”临床化学和临床药理学研究所所长兼 ImmunoSensation2 卓越集群发言人 Gunther Hartmann 教授解释说。“这导致人类免疫细胞中激酶 IKKepsilon 的持续降解。”
因此,TBK1 表达的缺失导致 IKKepsilon 的丰度增加。这种机制确保即使没有 TBK1 也能发生抗病毒免疫反应。另一方面,由点突变引起的 TBK1 功能丧失并不能阻止 IKKepsilon 的不稳定和降解,因此最终这两个因素都无法用于病毒防御。结果是对病毒感染的易感性增加。
病毒的武器
因此,在健康的生物体中,增加 IKKepsilon 的量可以补偿 TBK1 的损失。当病毒专门寻求消除人体自身的防御时,这一点就变得尤为重要。单纯疱疹病毒 1 (HSV-1)、人类免疫缺陷病毒 (HIV) 以及严重急性呼吸系统综合症冠状病毒 2 (SARS-CoV-2) 都能够特异性诱导 TBK1 降解。此外,一些细菌种类能够引起 TBK1 的降解。“我们的数据清楚地表明,人类免疫细胞具有重要的后备机制,”Wegner 博士解释说。“即使发生病原体诱导的 TBK1 降解,它们也能够维持有效的抗病毒反应。此外,该机制在 TBK1 遗传丢失的情况下也会起作用。”
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
